Kelarutan dan Hasil Kali Kelarutan
Sintesi
TLDRThe video explains the solubility of table salt (NaCl) in water, discussing how it dissociates into ions when dissolved. It describes the concept of saturation, including unsaturated, saturated, and supersaturated solutions. It also introduces the concept of the solubility product constant (Ksp) as it applies to salts in a saturated solution and provides examples for calculating solubility. Factors that affect solubility, such as temperature and the size of the solute particles, are also mentioned, emphasizing that temperature can increase the rate of dissolution.
Punti di forza
- 🧂 The solubility of salt depends on several factors.
- 💧 Salt dissolves and dissociates into ions in water.
- 📈 Saturated solutions cannot dissolve additional solute.
- 🧮 The solubility product constant (Ksp) helps calculate solubility.
- ℹ️ Different salts have different solubility behaviors.
- 🌡️ Temperature affects solubility, often increasing it.
- 🔍 Smaller particles dissolve faster than larger ones.
- 👩🔬 Ag2S·CrO4 serves as a calculation example for Ksp and solubility.
Linea temporale
- 00:00:00 - 00:09:07
The video begins with an experiment involving kitchen salt (NaCl) and water (H2O) to explore the solubility of salt in water. It explains that when a small amount of salt is added to water, it dissolves and dissociates into ions. As more salt is added, a point is reached where no more salt can dissolve, resulting in a saturated solution. This leads to the concept of solubility, defined as the maximum amount of salt that can dissolve in a given amount of water, categorizing solutions into unsaturated, saturated, and supersaturated. The video also discusses the solubility of different salts, noting that some dissolve easily while others, like silver chloride, do not. It introduces the solubility product constant (Ksp) and explains how to calculate the solubility of salts based on their dissociation in water, using examples to illustrate the relationship between solubility and Ksp. Finally, it mentions factors affecting solubility, such as temperature and the size of the solute particles, encouraging viewers to engage with the content by commenting and subscribing.
Mappa mentale
Video Domande e Risposte
What is the solubility of salt in water?
The solubility of salt varies; some dissolve easily while others do not. For example, sodium chloride is highly soluble, while silver chloride is less so.
What happens when you exceed the solubility of salt?
If you add more salt than can dissolve, it will not dissolve and will settle at the bottom as a crystal deposit.
What are the three types of solutions based on solubility?
The three types of solutions are unsaturated (can dissolve more solute), saturated (cannot dissolve more solute), and supersaturated (contains more solute than it normally can hold).
How is solubility expressed?
Solubility is expressed as the maximum amount of solute that can dissolve in a given volume of solvent, often in moles per liter (mol/L).
What factors affect the solubility of a solute?
Factors include temperature, the size of solute particles, the volume and type of solvent, and the speed of stirring.
What is the solubility product constant (Ksp)?
Ksp is a constant that describes the equilibrium between a solid and its ions in a saturated solution, allowing calculations of solubility.
Visualizza altre sintesi video

The UNHINGED Manifestation Method That Got My Ex Back | Neville Goddard Teaching

10 People Who Altered History as Entrepreneurs

The role of business in history: From merchants to entrepreneurs #entrepreneurship #historylessons

Are We Automating Racism?
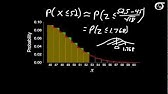
The Normal Approximation to the Binomial Distribution

Why you’re probably not doing your “dream job”
- solubility
- NaCl
- water
- saturated solution
- Ksp
- unsaturated
- supersaturated
- ionization
- factors affecting solubility
- chemistry